Was bedeutet Informed Consent?
Definition und rechtlicher Rahmen
Daten, die während eines Krankenhausaufenthalts oder einer ambulanten Behandlung erhoben werden, sind für die medizinische Forschung äußerst nützlich. Bevor auf Gesundheitsdaten zugegriffen werden kann, muss der Patient oder die Patientin aber schriftlich einwilligen. Diese Einwilligung wird auch als Informed Consent (informierte Einwilligung) bezeichnet. Die Daten dürfen ausschließlich für die darin beschriebene medizinische Forschung verwendet werden. Dabei müssen die Bestimmungen der DSGVO eingehalten werden – die Abkürzung steht für Datenschutz-Grundverordnung, eine Verordnung der Europäischen Union zur Verarbeitung personenbezogener Daten.
Informed Consent ist dazu nicht nur ein datenschutzrechtliches Erfordernis, sondern auch eine ethische Verpflichtung, unter anderem verankert im Arzneimittelgesetz. Für die Verarbeitung von Gesundheitsdaten gilt die DSGVO als Rechtsgrundlage.
Warum ist Einwilligung in Studien so wichtig?
Das Schöne ist, dass wir von Krankheiten lernen können. Doch wie funktioniert das Forschen mit Daten? Durch große Datenmengen lassen sich Muster erkennen, die bisher unbekannt waren. Diese erlauben Rückschlüsse auf Ursachen, Entstehungsgeschichten und den Verlauf von Krankheiten. Die Masse der Daten erlaubt es außerdem, Behandlungsmethoden miteinander zu vergleichen. So können bestehende Krankheiten und ihre Behandlungs- und Heilungsprozesse die Forschung durch ihre Daten „füttern“. Diese Forschung ist die Voraussetzung für eine evidenzbasierte, also auf wissenschaftliche Beweise gestützte Medizin. Digitale Einwilligung ermöglicht präzise Nachvollziehbarkeit und unterstützt die Forschung im Rahmen der Good Clinical Practice (ICH-GCP)-Standards. Sie ist Voraussetzung für die Zulässigkeit jeder klinischen oder epidemiologischen Studie in Europa.
Digitale Einwilligung (eConsent) – Chancen und Herausforderungen
Vorteile digitaler Einwilligungsprozesse
Die rasante technologische Entwicklung bei der Datenverarbeitung ermöglicht die allgemeine Digitalisierung im Gesundheitswesen. Die Einführung der elektronischen Patientenakte (ePA), der elektronischen Rezepte sowie der telemedizinischen Angebote profitiert von der Vernetzung der Daten. Digitale Prozesse sind schneller, leichter handhabbar, besser einsehbar und auch auffindbar als konventionelle. Das gilt auch für die Einwilligung in die Nutzung der Gesundheitsdaten. Selbst im Falle eines Widerrufs der Zustimmung ist der digitale Prozess von Vorteil, da zügig und gezielt gehandelt werden kann. Moderne eConsent-Systeme können zusätzlich digitale Identitätsnachweise (z. B. eID) integrieren und über Mobile-Health-Anwendungen eingebunden werden. Das erleichtert Einwilligungsprozesse bei dezentralen klinischen Studien (DCT) erheblich.
Transparenz und Nachvollziehbarkeit erhöhen
Vor einer Datennutzung durch die Gesundheitsforschung muss der Patient oder die Patientin eine digitale Einwilligung geben (eConsent). Mit der Einwilligungserklärung erhält man Patienteninformationen, die auf die Vorteile und Risiken der Nutzung von Daten hinweisen und somit den Prozess transparent und nachvollziehbar machen. Diese Formulare sollten aufmerksam gelesen werden, bevor man seine Daten für medizinische Studien zur Verfügung stellt. Die Transparenz der Datennutzung ist ein zentrales Element der Einwilligung. Innovative Lösungen setzen auf multimediale Inhalte (Videos, Infografiken) sowie interaktive Wissens-Checks, um sicherzustellen, dass die Teilnehmenden den Inhalt verstehen – ein zentraler Punkt der Qualitätsstandards für Informed Consent.
Technische Umsetzung: Digitale Unterschrift und Audit Trail
Die digitale Unterschrift ersetzt die handschriftliche Signatur rechtssicher – sie kann z. B. mit Zwei-Faktor-Authentifizierung kombiniert werden. Für Studien ist der sogenannte Audit Trail entscheidend: Jede Änderung der Einwilligung wird mit Zeitstempel dokumentiert. So bleibt der Einwilligungsprozess nachvollziehbar, revisionssicher und DSGVO-konform. Zusätzlich ist ein Audit Trail nach ICH-GCP zwingend erforderlich: Alle Änderungen, Widerrufe und Zugriffe müssen manipulationssicher dokumentiert werden. Bei Softwarelösungen gilt die Validierungspflicht nach MDR (Medizinprodukterecht), falls sie als Medizinprodukt klassifiziert werden.
Datenschutz & DSGVO bei der Einwilligung
Anforderungen der DSGVO
Für die Einwilligungserklärung gilt das europäische Datenschutzrecht, sie muss daher mit den Bestimmungen der DSGVO konform gehen. Dies beinhaltet die sogenannte Rechenschaftspflicht der Forschung, die mit Patientendaten arbeitet. Das bedeutet, die Einwilligung muss nachweisbar sein: Die Verarbeitung der personenbezogenen Daten muss dokumentiert werden. Sie muss außerdem eine klare Zweckbindung enthalten; es darf keine Pauschaleinwilligung sein. Studien müssen zudem die Kontaktdaten des Datenschutzbeauftragten nennen. Und Nutzer sind verpflichtet, eConsent-Systeme datenschutzfreundlich zu konzipieren.
Die verantwortliche Organisation muss auf Nachfrage der Aufsichtsbehörde belegen können, dass die Vorgaben der DSGVO erfüllt wurden. Dabei sollte eine Einwilligungserklärung verständlich formuliert sein und vor der Datennutzung abgeschlossen werden.
Umgang mit sensiblen Gesundheitsdaten
Gesundheitsdaten unterstehen dem Persönlichkeitsrecht, deshalb unterstehen diese sensiblen Daten einem besonderen Schutz. Gemäß den Vorschriften der DSGVO müssen sie mit großer Sorgfalt behandelt werden, um die Privatsphäre der behandelten Personen zu wahren.
Die DSGVO hat dazu Schutzmechanismen etabliert, die die Verarbeitung dieser Informationen regulieren. Dazu gehören strenge Vorschriften für die Speicherung und Übermittlung der Daten. Ein zentraler Aspekt ist die Pseudonymisierung oder Anonymisierung von Daten, um eine Identifizierung von Personen zu verhindern. Zudem müssen Organisationen Sicherheitsmaßnahmen implementieren, um Daten vor unbefugtem Zugriff oder Missbrauch zu schützen.
Für Sekundärnutzung und Big-Data-Forschung fordert die EU zunehmend Trusted Research Environments (TRE) oder Datentreuhänder, um Anonymisierung und Zugangskontrolle sicherzustellen. Dies ist Teil des European Health Data Space (EHDS), der ab 2025 umgesetzt wird.
Rechte der Teilnehmenden: Widerruf und Löschung
Die Einwilligung ist freiwillig und hat keinen Einfluss auf die Behandlung. Teilnehmende, die ihre Einwilligung gegeben haben, können sie jederzeit widerrufen. Die gespeicherten Daten werden dann automatisch umgehend gelöscht.
Best Practices für digitale Einwilligungsprozesse
Digitale Einwilligungsformulare sollten modular aufgebaut sein: mit interaktiven Elementen, übersichtlicher Navigation, mehrsprachigen Inhalten und integrierter Widerrufsfunktion. Tools wie D4L Collect ermöglichen dies in rechtssicherer Weise.
Was gehört in eine Einwilligungserklärung?
Die Einwilligung muss ausdrücklich für einen oder mehrere Zwecke erteilt, also zweckgebunden gegeben werden. Der betroffenen Person muss erklärt werden, wozu ihre personenbezogenen Daten genutzt werden könnten. Dabei muss die Freiwilligkeit der Unterzeichnung unterstrichen, ein Widerrufsrecht der Einwilligung ausdrücklich erwähnt werden. Es darf kein Nachteil für die zu behandelnde Person durch den Widerruf entstehen.
Aufklärungspflichten ethisch korrekt erfüllen
Die Forschungsvorhaben, die Daten nutzen, werden jeweils von einer unabhängigen Ethikkommission geprüft. Nach einer zustimmenden Bewertung dieses Gremiums dürfen die Daten ausschließlich im Rahmen der Einwilligung für die medizinische Forschung genutzt werden. Die Forschungsvorhaben müssen den Patient:innen nachvollziehbar erklärt werden. Der jederzeit mögliche Widerruf der Einwilligung gehört zur Aufklärungspflicht und muss hinreichend beschrieben werden.
Sobald die Einwilligung nach medizinischem Ethikrecht erteilt ist, werden die Daten der Patienten anonymisiert, Name und Wohnort werden verschlüsselt, also durch Codes ersetzt, um die Privatsphäre zu schützen. Dadurch ist kein Rückschluss auf die Person möglich. Die codierten Daten werden danach an Universitäten, Forschungsunternehmen und -institute weitergeleitet.
Praxisbeispiele und Formulierungshilfen
Zum Beispiel können Forscher eine Blutprobe vielfältig untersuchen: Es können Laborwerte gemessen, Krankheitserreger nachgewiesen und genetische Daten analysiert werden. Es könnten auch Hinweise auf zusätzliche Krankheiten entdeckt werden. Mit den Daten kann die medizinische Forschung neue Therapien entwickeln.
Für Unternehmen, Institute und Universitäten, die Einwilligungserklärungen formulieren wollen, gibt es online gute Formulierungshilfen. So bietet beispielsweise die Medizin-Informatik-Initiative Mustertexte auf ihrer Webseite an – auf türkisch, englisch und deutsch. EU-Leitfäden wie „Guidelines on consent for scientific research under GDPR“ liefern zusätzliche Orientierung.
Zukunftsausblick: eConsent in der Gesundheitsforschung
Wearables und Mobile Health Apps erzeugen kontinuierlich Gesundheitsdaten. Die Integration von eConsent in solche digitalen Ökosysteme wird immer wichtiger. Plattformen müssen interoperabel sein, um Datensätze aus unterschiedlichen Quellen zusammenzuführen – etwa aus Kliniksystemen, Patienten-Apps oder Biobanken.
Interoperabilität
In der Praxis zeigt sich, dass Interoperabilität von entscheidender Bedeutung ist. Sowohl bei der Datenerhebung als auch bei der Datenverarbeitung und -analyse sind Standards das A und O, um die Arbeit mit ihnen möglich zu machen. Der FHIR-Standard eignet sich für die Datenerhebung, in der Forschung wird der OMOP-Standard erfolgreich angewandt. Und die beiden können zusammengeführt werden - was eine zentrale Anforderung ist. Auf der Grundlage der FAIR-Prinzipien (Findable, Accessible, Interoperable, Reusable) können Gesundheitsdaten dann mehrsprachig für diverse Studienpopulationen erhoben werden
Nachhaltigkeit und Vertrauen durch digitale Lösungen
Digitale Lösungen, um Daten zu gewinnen, auszuwerten und rechtlichen Anforderungen zu genügen, eröffnen unzählige neue Möglichkeiten. Schnelligkeit, Genauigkeit und unbürokratische Arbeitsweise versprechen, dass neue medizinische Erkenntnisse deutlich zügiger gewonnen werden können. Die kurzen und ressourcenknappen Wege sind dazu nachhaltiger. Auch die direkte Überprüfbarkeit sowohl für Anbieter als auch die Patient:innen fördert das Vertrauen in die Zusammenarbeit.
Für den grenzüberschreitenden Datenaustausch in Europa ist die Umsetzung des EHDS (European Health Data Space) und die Blockchain-Technologie entschieden hilfreich, für eine manipulationssichere Nachvollziehbarkeit zu sorgen.
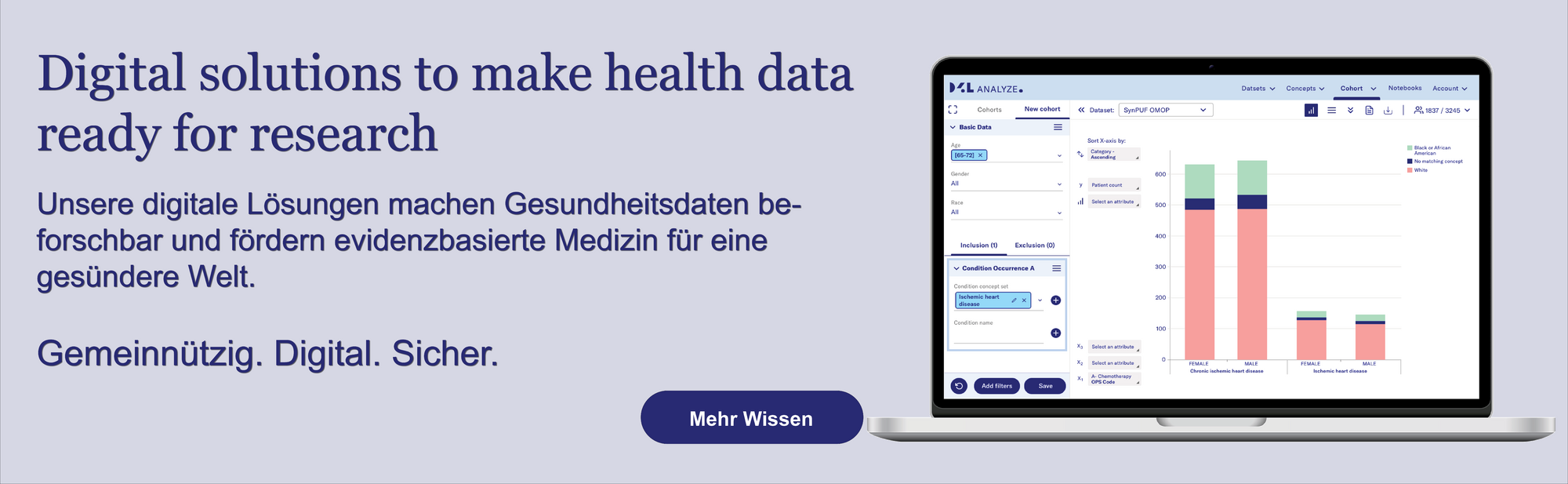
Die digitalen Lösungen von Data4Life machen Gesundheitsdaten beforschbar und fördern evidenzbasierte Medizin.
Die Inhalte dieses Artikels geben den aktuellen wissenschaftlichen Stand zum Zeitpunkt der Veröffentlichung wieder und wurden nach bestem Wissen und Gewissen verfasst. Dennoch kann der Artikel keine medizinische Beratung und Diagnose ersetzen. Bei Fragen wenden Sie sich an Ihren Allgemeinarzt.
Ursprünglich veröffentlicht am